Nội dung:
- 1 Thiết Bị Y Tế Là Gì? Định Nghĩa Theo Tiêu Chuẩn Quốc Tế
- 2 Tại Sao Thiết Bị Y Tế Cần Gắn Dấu CE?
- 3 Quy Định Về Thiết Bị Y Tế Theo Châu Âu (Chỉ Thị MDD)
- 4 Phân Loại Thiết Bị Y Tế Theo Mức Độ Rủi Ro
- 5 Quy Trình Gắn Dấu CE Cho Thiết Bị Y Tế
- 6 Đánh Giá Hồ Sơ Kỹ Thuật và Hệ Thống Chất Lượng
- 7 Lợi Ích Khi Thiết Bị Y Tế Có CE Marking
- 8 Đơn Vị Hỗ Trợ Về Chứng Nhận CE: GCDRI Đồng Hành Cùng Doanh Nghiệp
- 9 Kết Luận
Để các sản phẩm thiết bị y tế được phép lưu hành tại thị trường châu Âu, nhà sản xuất bắt buộc phải đáp ứng các yêu cầu nghiêm ngặt được quy định trong Chỉ thị 93/42/EEC của EU – thường được gọi là chỉ thị MDD (Medical Devices Directive). Từ đó, việc gắn dấu CE trở thành điều kiện tiên quyết để chứng minh sự phù hợp về an toàn và hiệu quả của sản phẩm trong hoạt động chăm sóc sức khỏe.
Trong bài viết chuyên sâu này, Viện Nghiên Cứu Phát Triển Chứng Nhận Toàn Cầu (GCDRI) sẽ cung cấp cho bạn cái nhìn toàn diện và cập nhật nhất về dấu CE dành cho thiết bị y tế – từ khái niệm, lý do cần thiết, tiêu chí phân loại đến quy trình đánh giá, chứng nhận và quyền lợi đi kèm.
Thiết Bị Y Tế Là Gì? Định Nghĩa Theo Tiêu Chuẩn Quốc Tế
✍️ Tìm hiểu thêm: Khái niệm dấu CE đồ chơi là gì | Tác dụng và quy trình
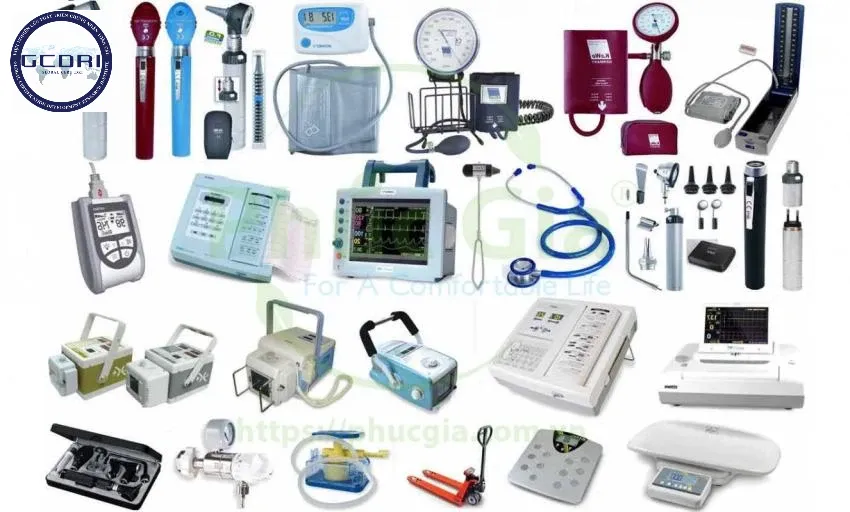
Định nghĩa về thiết bị y tế có thể khác nhau tùy theo từng quốc gia, nhưng về cơ bản, thiết bị y tế được hiểu là bất kỳ dụng cụ, thiết bị, phần mềm, vật liệu hoặc sản phẩm nào được sử dụng cho mục đích chuẩn đoán, điều trị, theo dõi, phòng ngừa bệnh tật hoặc hỗ trợ chức năng sinh lý cho con người mà không sử dụng cơ chế dược lý.
Theo định nghĩa của Tổ chức Y tế Thế giới (WHO), thiết bị y tế bao gồm:
- Các thiết bị đơn giản như băng urgo, nẹp cố định
- Thiết bị phẫu thuật như dao, kéo, máy laser
- Máy móc chẩn đoán hình ảnh như máy siêu âm, máy chụp X-quang
- Hệ thống hỗ trợ sự sống như máy điều hòa nhịp tim, máy thở
Lưu ý: Những sản phẩm có tác dụng điều trị dựa trên phản ứng hóa học hoặc thay đổi sinh lý (thuốc, vắc xin, mỹ phẩm,…) – dù có ứng dụng y tế – sẽ không được phân loại là thiết bị y tế và phải tuân thủ các quy định khác.
Tại Sao Thiết Bị Y Tế Cần Gắn Dấu CE?

✍️ Tìm hiểu thêm: Tư vấn chứng nhận CE thép và nhôm | Sản phẩm kết cấu kiện Thép – Nhôm
Dấu CE (Conformité Européenne) không chỉ là biểu tượng pháp lý giúp các sản phẩm được lưu thông tự do tại khu vực Kinh tế châu Âu (EEA), mà còn là “giấy thông hành” khẳng định rằng sản phẩm tuân thủ đầy đủ các yêu cầu an toàn và hiệu quả của pháp luật EU.
Đối với thiết bị y tế, dấu CE đặc biệt quan trọng vì:
- Là bằng chứng sản phẩm được sản xuất và kiểm soát theo quy chuẩn kỹ thuật nghiêm ngặt
- Tạo niềm tin cho các cơ quan y tế, nhà phân phối và người tiêu dùng
- Là điều kiện bắt buộc để được lưu hành tại EU
- Mở cánh cửa gia nhập vào thị trường các quốc gia đang thừa nhận CE trong hệ thống quản lý chất lượng
Quy Định Về Thiết Bị Y Tế Theo Châu Âu (Chỉ Thị MDD)
✍️ Tìm hiểu thêm: Tại sao cần chứng nhận CE để xuất khẩu Châu Âu | Giải thích chi tiết
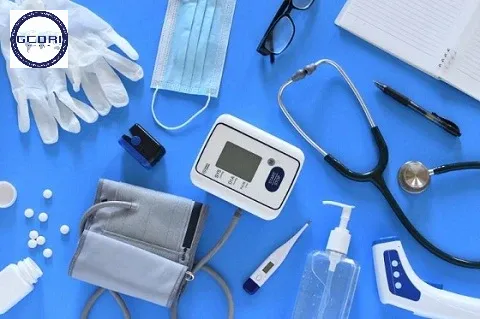
Chỉ thị 93/42/EEC là văn bản pháp lý nền tảng quy định các yêu cầu đối với thiết bị y tế tại châu Âu. Khi áp dụng chỉ thị này, các doanh nghiệp cần đảm bảo sản phẩm tuân thủ đầy đủ các nội dung sau:
- An toàn cho người sử dụng và bệnh nhân
- Hiệu năng sản phẩm phù hợp mục đích sử dụng
- Tính tương thích sinh học
- Kiểm soát rủi ro trong thiết kế và sản xuất
Chỉ thị MDD cũng yêu cầu các doanh nghiệp phải đưa ra bằng chứng kỹ thuật, thực hiện các thử nghiệm cần thiết và kiểm soát chuỗi sản xuất trước khi tuyên bố sản phẩm phù hợp để gắn dấu CE.
Phân Loại Thiết Bị Y Tế Theo Mức Độ Rủi Ro
Việc xác định đúng loại thiết bị là yếu tố tiên quyết trong quy trình CE Marking vì mỗi nhóm (class) có yêu cầu tuân thủ và cách đánh giá khác nhau. Trong chỉ thị MDD, thiết bị y tế được phân loại theo 4 nhóm cơ bản:
- Class I (Nguy cơ thấp): băng gạc, túi nhiệt,…
- Class IIa (Nguy cơ trung bình – thấp): thiết bị hô hấp, ống nội soi
- Class IIb (Nguy cơ trung bình – cao): máy thẩm tách máu, máy hô hấp chức năng
- Class III (Nguy cơ cao): máy trợ tim, van tim nhân tạo,…
Việc xếp loại dựa trên các yếu tố như:
- Mức độ xâm lấn vào cơ thể
- Thời gian sử dụng liên tục
- Tác động đến sinh lý người bệnh
- Mức độ phụ thuộc vào phần mềm hoặc điện tử
Phần lớn thiết bị từ Class II trở lên sẽ bắt buộc phải đánh giá bởi các Tổ chức được chỉ định (Notified Bodies). Càng rủi ro cao, quy trình chứng nhận và kiểm định càng nghiêm ngặt.
Quy Trình Gắn Dấu CE Cho Thiết Bị Y Tế
Việc đạt chứng nhận CE không đơn giản là chỉ dán nhãn lên thiết bị. Đó là một quy trình kiểm định hệ thống và sản phẩm toàn diện gồm nhiều bước bắt buộc:
1. Xác định Yêu Cầu Của EU
Doanh nghiệp cần xác định rõ các quy định pháp lý và tiêu chuẩn điều chỉnh sản phẩm y tế cụ thể trong từng nhóm nguy cơ.
2. Phân Loại Sản Phẩm Đúng Mức Rủi Ro
Dựa trên phân loại tại chỉ thị MDD, xác định lớp thiết bị y tế để lựa chọn quy trình đánh giá phù hợp.
3. Chuẩn Bị Hồ Sơ Kỹ Thuật
Thiết lập hồ sơ kỹ thuật (Technical Documentation) bao gồm:
- Mô tả sản phẩm
- Hướng dẫn sử dụng
- Kết quả thử nghiệm
- Phân tích rủi ro
- Chứng nhận hệ thống chất lượng ISO 13485 (nếu có)
4. Đánh Giá Sự Phù Hợp
Tuỳ mức phân loại thiết bị, doanh nghiệp sẽ tự công bố hoặc phải thông qua tổ chức chứng nhận bên ngoài. Chứng nhận có thể theo các phụ lục:
- Phụ lục II: Đánh giá đầy đủ hệ thống chất lượng
- Phụ lục IV: Kiểm nghiệm mẫu hoặc từng lô sản phẩm cụ thể
- Phụ lục V & VI: Đánh giá sản xuất hoặc kiểm soát cuối
5. Gắn Dấu CE và Tuyên Bố Phù Hợp
Sau khi đánh giá thành công và có chứng nhận, doanh nghiệp ban hành Bản tuyên bố phù hợp EU (EU Declaration of Conformity) và gắn dấu CE lên thiết bị, bao bì hoặc tài liệu kỹ thuật đi kèm.
Lưu ý: Đối với thiết bị vô trùng hoặc có chức năng đo lường, CE phải kèm theo mã số Notified Body.
Đánh Giá Hồ Sơ Kỹ Thuật và Hệ Thống Chất Lượng
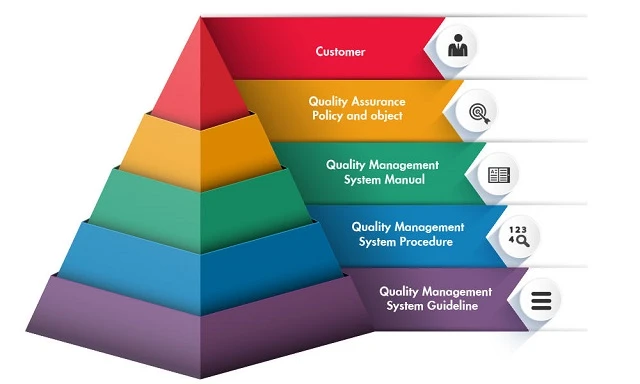
Để sản phẩm được gắn CE, doanh nghiệp cần xây dựng hệ thống quản lý chất lượng đạt chuẩn quốc tế như:
- ISO 13485:2016 – Tiêu chuẩn hệ thống QLCL cho thiết bị y tế
- Quy trình quản lý rủi ro theo ISO 14971:2019
Tổ chức chứng nhận sẽ xem xét hồ sơ, thử nghiệm sản phẩm và đánh giá trực tiếp hệ thống tại nhà máy nếu cần.
✍️ Tìm hiểu thêm: Dịch vụ cấp chứng nhận CE tại Hà Nội và TPHCM
Lợi Ích Khi Thiết Bị Y Tế Có CE Marking
Chứng nhận CE không chỉ giúp thiết bị được lưu hành hợp pháp tại châu Âu, mà còn mang lại nhiều giá trị thiết thực:
- Tăng uy tín thương hiệu doanh nghiệp trong mắt khách hàng, đối tác và nhà đầu tư
- Mở rộng khả năng xuất khẩu sang thị trường EU và các quốc gia công nhận CE như UAE, Thổ Nhĩ Kỳ,…
- Giảm thiểu rủi ro pháp lý khi bị kiểm tra hoặc xử lý hậu kiểm
- Tăng sự tín nhiệm từ cơ sở y tế và chuyên gia chăm sóc sức khỏe
Đơn Vị Hỗ Trợ Về Chứng Nhận CE: GCDRI Đồng Hành Cùng Doanh Nghiệp
Với đội ngũ chuyên gia lâu năm trong lĩnh vực nghiên cứu và tư vấn chứng nhận quốc tế, GCDRI mang lại:
- Phân tích chi tiết yêu cầu pháp lý đối với từng sản phẩm
- Hướng dẫn xây dựng hồ sơ kỹ thuật và hệ thống quản lý phù hợp
- Đại diện làm việc với các Notified Bodies uy tín tại EU
- Đồng hành trọn gói từ đánh giá ban đầu đến khi sản phẩm được gắn dấu CE và lưu hành thành công
Kết Luận
Tư vấn cấp chứng nhận CE Marking là bước đi chiến lược không thể thiếu nếu doanh nghiệp muốn đưa thiết bị y tế ra thị trường châu Âu. Ngoài việc đảm bảo sự tuân thủ pháp lý, chứng nhận CE còn là cam kết về chất lượng và an toàn với cộng đồng. Để quy trình đạt hiệu quả và tiết kiệm chi phí, lựa chọn một đơn vị tư vấn giàu kinh nghiệm như GCDRI là giải pháp lý tưởng.
Hãy để Viện Nghiên Cứu Phát Triển Chứng Nhận Toàn Cầu trở thành đối tác tin cậy trong hành trình quốc tế hóa sản phẩm thiết bị y tế của bạn.
Liên hệ ngay Hotline: 0904.889.859 (Ms.Hoa) hoặc email: chungnhantoancau@gmail.com để được tư vấn chuyên sâu và hỗ trợ khởi động quy trình chứng nhận CE cho thiết bị y tế của doanh nghiệp bạn.
Hoa Linh là chuyên gia tư vấn và triển khai hệ thống quản lý theo tiêu chuẩn quốc tế ISO với hơn 8 năm kinh nghiệm hỗ trợ doanh nghiệp Việt Nam đạt chứng nhận ISO 9001, ISO 14001, ISO 45001, ISO 22000, ISO 27001 và ISO 50001. Với nền tảng kiến thức chuyên sâu về quản lý chất lượng, quản lý môi trường, an toàn lao động và an toàn thông tin, Hoa Linh đã đồng hành cùng hàng trăm doanh nghiệp trong đa dạng lĩnh vực như sản xuất, thực phẩm, logistics, xây dựng, dịch vụ thương mại và công nghệ. Khả năng phân tích hệ thống hiện tại của doanh nghiệp, tư vấn các giải pháp cải tiến phù hợp, xây dựng tài liệu ISO chuyên nghiệp, đào tạo đội ngũ nhân sự, đánh giá nội bộ và hỗ trợ doanh nghiệp làm việc với tổ chức chứng nhận quốc tế.
Hiện tại, Hoa Linh là chuyên gia của Viện Nghiên Cứu Phát Triển Chứng Nhận Toàn Cầu (GCDRI) và trực tiếp tham gia tư vấn - đào tạo - hỗ trợ doanh nghiệp đạt chứng nhận ISO theo yêu cầu của khách hàng và đối tác quốc tế.
Like fanpage GCDRI để nhận tin mới mỗi ngày!





